Ausgleichen chemischer Gleichungen
Chemie ist, wenn zwei Stoffe miteinander reagieren und sich zu neuen Stoffen verbinden.
Mischt man Wasserstoffgas mit Sauerstoff, so reagieren diese in einer heftigen Reaktion (Knallgasreaktion) zu Wasser. Verbrennt man Kohlenstoff, so verbindet sich dieser mit Sauerstoff und Kohlenstoffdioxid entweicht.
Wie viel aber benötigt man genau von jedem Stoff? In welchem Verhältnis muss man Wasserstoff mit Sauerstoff mischen, damit möglichst viel Produkt entsteht und möglichst wenig Anfangsstoffe übrig bleiben?
GRUNDLAGEN
Bei chemischen Reaktionen bleibt die Anzahl der vorhandenen Atome je Element immer unverändert!
->Kein Atom verschwindet, keines kommt dazu!
Wichtig: Formeln darf man nie verändern! Aus O2 wird NIE O3, auch wenn es sich dann ausginge!
Ausgleichen einfacher chemischer Reaktionen
C |
+ |
02 |
-> |
CO2 |
 |
 |
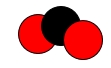 |
Das geht sich gut aus. Man muss nichts mehr weiter tun. Der Kohlenstoff verbrennt mit O2 zu CO2. Passt!
Wenn ein Molekül nur einmal vorkommt (1 C+1 O2), schreibt man vereinfacht nur C+O2
Was aber, wenn es sich nicht ausgeht? H2 und O2 reagieren ja nicht zu H2O2 (Wasserstoffperoxid) sondern zu H2O, dem Wasser:
Kompliziertere Fälle
H2 |
+ |
O2 |
-> |
H2O |
|
|
+ |
|
-> |
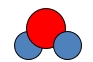 |
Das geht sich nicht aus. Man hat ja links 2 O Atome, rechts (im Produkt) nur eines.
Man muss nun auf beiden Seiten die Atome bzw. Teilchen so multiplizieren, dass die Anzahl der Atome der beteiligten Elemente auf beiden Seiten des Gleichheitszeichens gleich ist.
Man sucht sich die einfachste, ohne Brüche darstellbare Möglichkeit. Als Zwischenschritt zur richtigen Lösung kann man vorübergehend mit Brüchen arbeiten, muss diese aber dann in ganze Zahlen verwandeln (weil halbe Moleküle gibt es nicht):
H2+ 1/2 O2-> H2O I x2
2H2+O2 -> 2H2O
Wenn ein Molekül nur einmal vorkommt, schreibt man z.B. nur H2. Man könnte aber auch 1H2 schreiben.
2H2 |
+ |
O2 |
-> |
2H2O |
|
|
+ |
|
-> |
|
Wichtig auch hier: Formeln darf man nie verändern! Aus O2 wird NIE O3, auch wenn sieh es dann ausginge! Und wenn H2O das Produkt ist, dann ist es H2O und nicht H2O2.[/
Silke Geroldinger
Quellen:
http://www.meerbusch-gymnasium.de/Fachschaften/FS_Chemie/uebungen/gleichungen_9.htm