Schrödinger Heisenberg Modell
Die Verbesserung und Weiterentwicklung des Bohrschen Atommodells ist die Orbitaltheorie.
Werner Heisenberg entwickelte mathematische Lösungen (=Unschärferelation). Diese
besagen, dass es unmöglich ist, den Ort und Impuls eines Teilchens gleichzeitig korrekt zu
bestimmen. Die festen Kreisbahnen im Bohrsehen Atommodell verwischten zu Bändern.
Erwin Schrödinger übernahm von Albert Einstein und Louis de Broglie die Idee, dass Lichtwellen auch Teilcheneigenschaften, Lichtquanten besitzen. Die Umkehrung dieser Annahme besagt, dass Materie auch über Welleneigenschaften verfügt.
Durch diese Annahmen entwickelte er 1927 die mathematische Erklärung (=Schrödinger-Gleichung). Louis de Broglie bestätigte die Annahme im selben Jahr durch Experimente.
Die Schrödinger-Gleichung gibt eine Verbindung zwischen Welleneigenschaften der Energie und den Ort des Elektrons.
Das Ergebnis ist die Aufenthaltswahrscheinlichkeit des Elektrons. Diese gibt Auskunft über die Raumelemente, in denen ein Elektron am häufigsten ist.
Es gibt unendlich viele Wellenfunktionen, davon sind allerdings nur einige bestimmte sinnvoll.
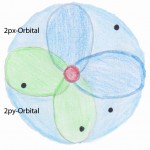
Die Aufenthaltswahrscheinlichkeit kann durch die Atomarbitale dargestellt werden. Diese erhält man durch die Wellenfunktion (=Eigenfunktion der Elektronen). Die Gesamtenergie des Elektrons darf nur bestimmte gequantelte Werte annehmen können .
Bericht von Julia Varga und Anna Mader, 1HGA, 2014
Quellen: http://elektroniktutor.de/grundlagen/a_modell.html
http://www.wissen.de/lexikon/orbitaltheorie
Schrödinger-Heisenberg Modell
Quiz-Zusammenfassung
0 von 7 Fragen beantwortet
Fragen:
- 1
- 2
- 3
- 4
- 5
- 6
- 7
Informationen
Wenn Du den Text aufmerksam gelesen hast, wirst Du die Fragen bestimmt korrekt beantworten können:
Sie haben das Quiz schon einmal absolviert. Daher können sie es nicht erneut starten.
Quiz wird geladen...
Sie müssen sich einloggen oder registrieren um das Quiz zu starten.
Sie müssen erst folgende Quiz beenden um dieses Quiz starten zu können:
Ergebnis
0 von 7 Frage korrekt beantwortet
Ihre Zeit:
Zeit ist abgelaufen
Sie haben 0 von 0 Punkten erreicht (0)
| Ø Punkte |
|
| Deine Punkte |
|
Kategorien
- Nicht kategorisiert 0%
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- Beantwortet
- Vorgemerkt
-
Frage 1 von 7
1. Frage
1 PunkteWas beschreibt die Schrödinger Gleichung?
- Die Schrödinger-Gleichung gibt eine Verbindung zwischen Welleneigenschaften der (Energie) und dem (Ort) des Elektrons.
Korrekt
Inkorrekt
-
Frage 2 von 7
2. Frage
1 PunkteDas Schrödinger Heisenberg Modell ist die Weiterentwicklung welchen Atom Modells?
Korrekt
Inkorrekt
-
Frage 3 von 7
3. Frage
1 PunkteWelche Idee über nahm Erwin Schrödinger von Albert Einstein und Louis de Broglie?
- Erwin Schrödinger übernahm von Albert Einstein und Louis de Broglie die Idee, dass Lichtwellen auch (Teilcheneigenschaften), Lichtquanten besitzen
Korrekt
Inkorrekt
-
Frage 4 von 7
4. Frage
1 PunkteWeie könnte man das Schrödinger Heisenberg noch nennen?
Korrekt
Inkorrekt
-
Frage 5 von 7
5. Frage
1 PunkteWann stellte Schrödinger seine Gleichung auf?
Korrekt
Inkorrekt
-
Frage 6 von 7
6. Frage
1 PunkteWelche Information gewinnt man durch die Schrödinger Gleichung?
- Die (Aufenthaltswahrscheinlichkeit) des Elektrons. Die Gleichung gibt Auskunft über die Raumelemente, in denen ein Elektron am häufigsten ist.
Korrekt
Inkorrekt
-
Frage 7 von 7
7. Frage
1 PunkteWie kann die Aufenthaltswahrscheinlichkeit dargestellt werden?
Korrekt
Inkorrekt
One comment
Schreibe einen Kommentar Antwort abbrechen
Diese Website verwendet Akismet, um Spam zu reduzieren. Erfahre mehr darüber, wie deine Kommentardaten verarbeitet werden.


Hallo Ihr angehenden Physiker
Wenn man dieses Reultat sieh, weis man das mit e= MC^2 gerechnet wurde.
Versucht es mal mit E=mc^2 pi und ihr werded stauenn
Gruss
Felix der Glückliche 🙂